3 min read
2020-Nature-A metabolic pathway for bile acid dehydroxylation
2022-05-21
为什么读这篇文章
- 计划把Michael A. Fischbach和Mohamed S. Donia 作为第一批post doc老板
- 这一篇是他们最近的一篇自己的文章
- 主要是偏化学和天然产物发现,以了解为主
Background
- 肠道微生物中有大量的代谢通路,但大部分的基因还没有被发现
- 肠道-小分子被研究的3个主要原因:
- 大部分或者完全由肠道微生物生成的小分子化合物可以进入循环系统,然后在周边组织和器官中发挥作用
- 它们的浓度与常见药物相近或者相似,并在不同人中有显著的差异,比如indoxyl sulfate
- 一些高丰度的小分子其生物学功能已经被完全理解,主要作用于宿主的关键受体,比如SCFA通过GPR41/GPR43作用免疫系统
- Cholic acid –> DCA (7α-dehydroxylation),CDCA到clithocholic acid (LCA)还原通路未知,本文通过纯化通路酶,确定了这个完整的还原通路,利用遗传手段体外重构通路进一步验证,然后通过菌群定植的方式展示出可以通过遗传手段来展示菌群治疗的可能性
Reconstitution of 7α-dehydroxylation
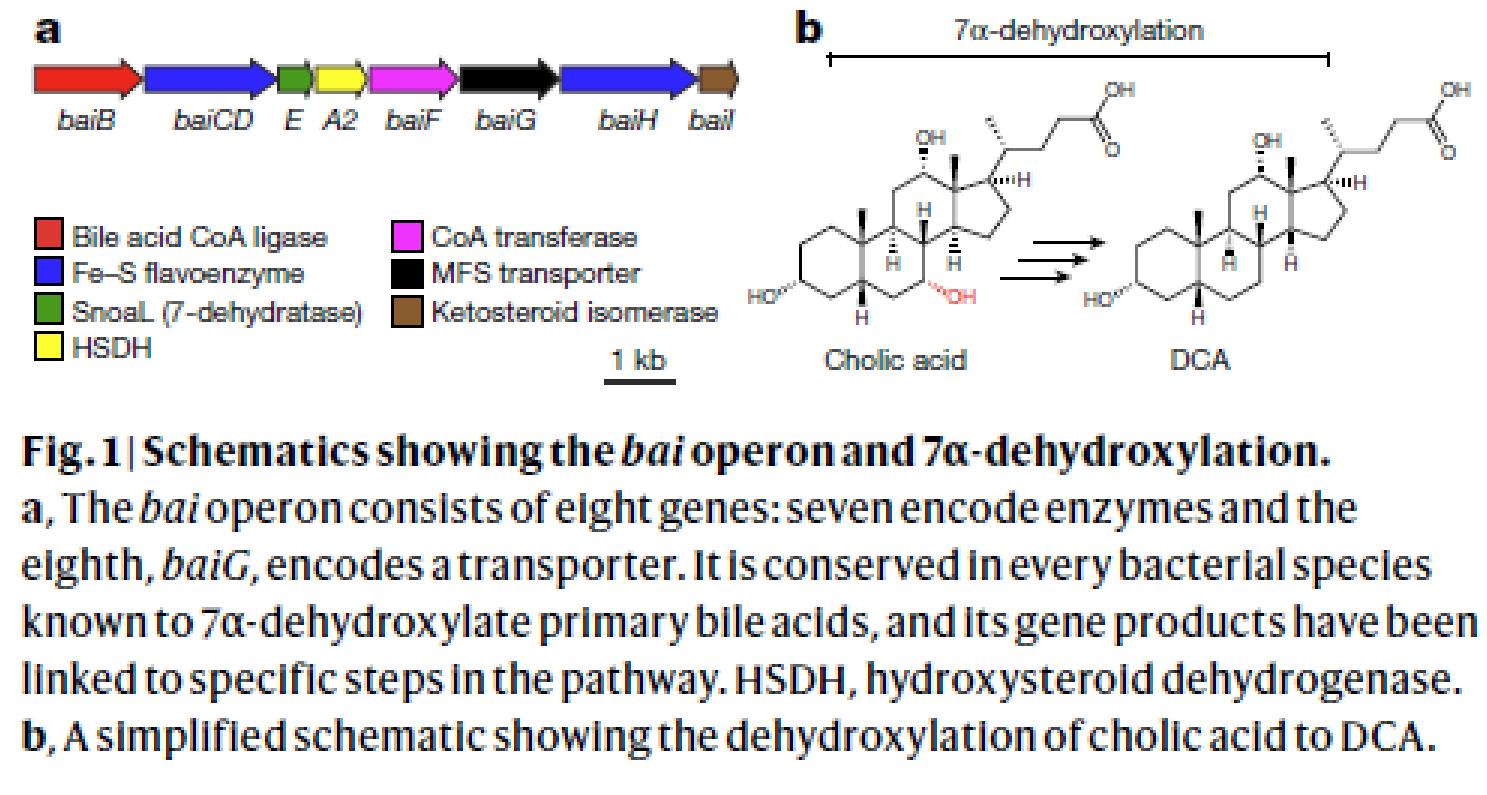
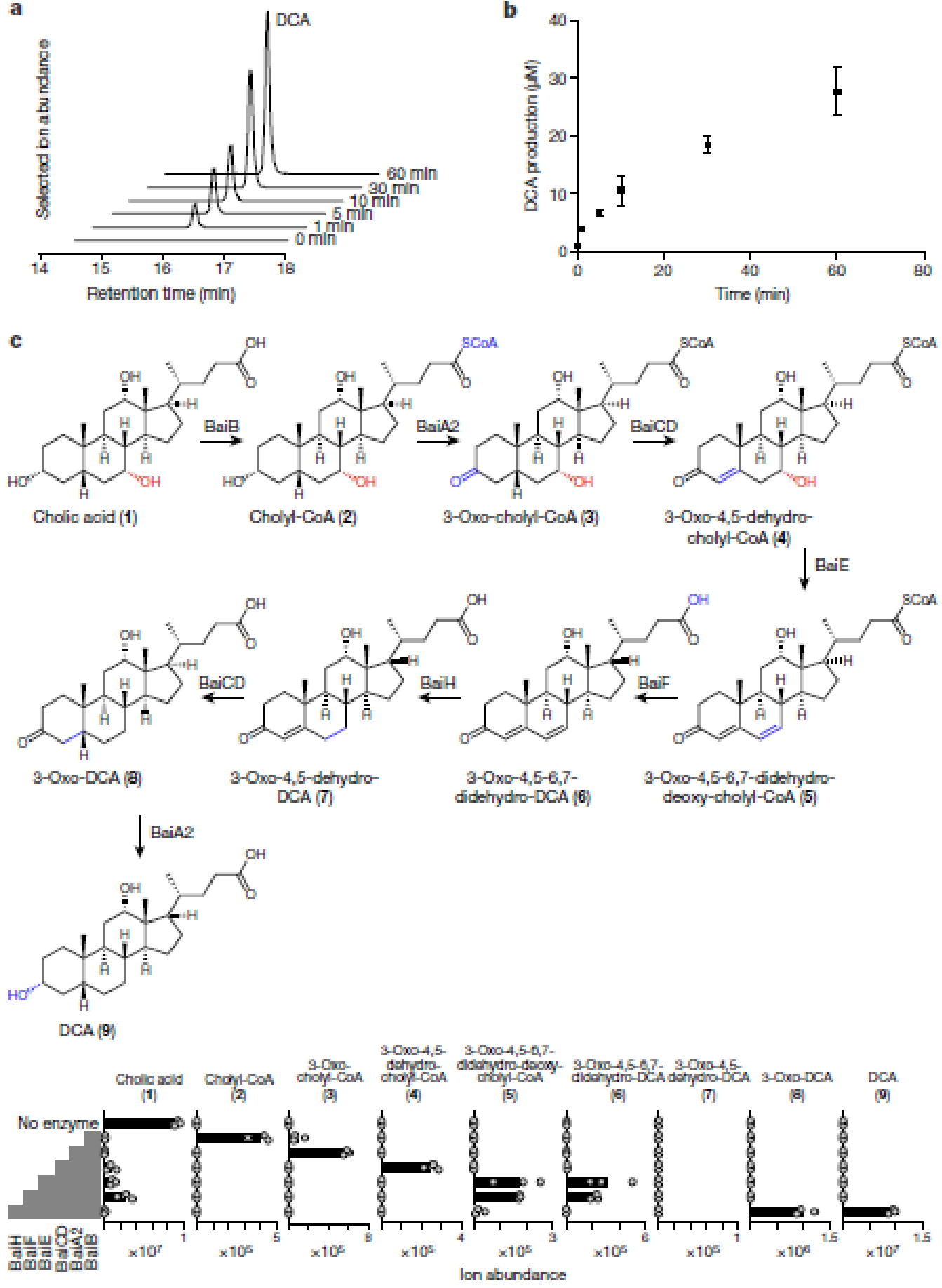
- 纯化出每一个bai操纵子中的酶,然后与cholic acid作用,证明这些酶能够发生7α-dehydroxylation,而不需要其他酶
- 进一步通过逐步加入每一个酶进行验证,LC-MS分析中间产物,表明每一个酶都是必要的
Engineering the pathway into C. sporogenes
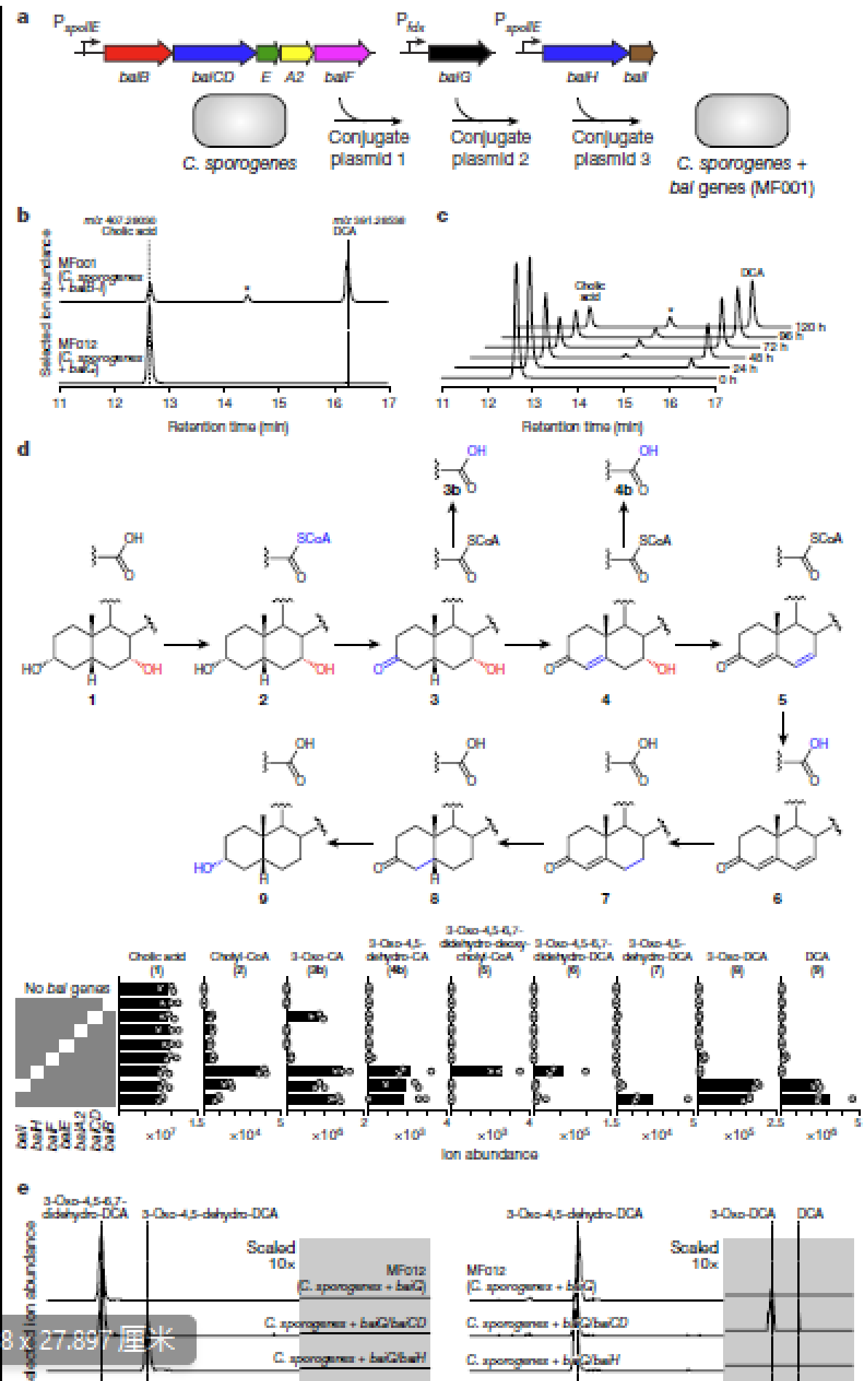
- 利用遗传学的方法将这一通路移植到产芽孢梭菌(C. sporogenes),这个也是之前没有做过的,具体的遗传学操作不是太懂,最终得到一个菌株MF001,从而使得MF001也具备了DCA的合成能力
Identifying branch points in the pathway
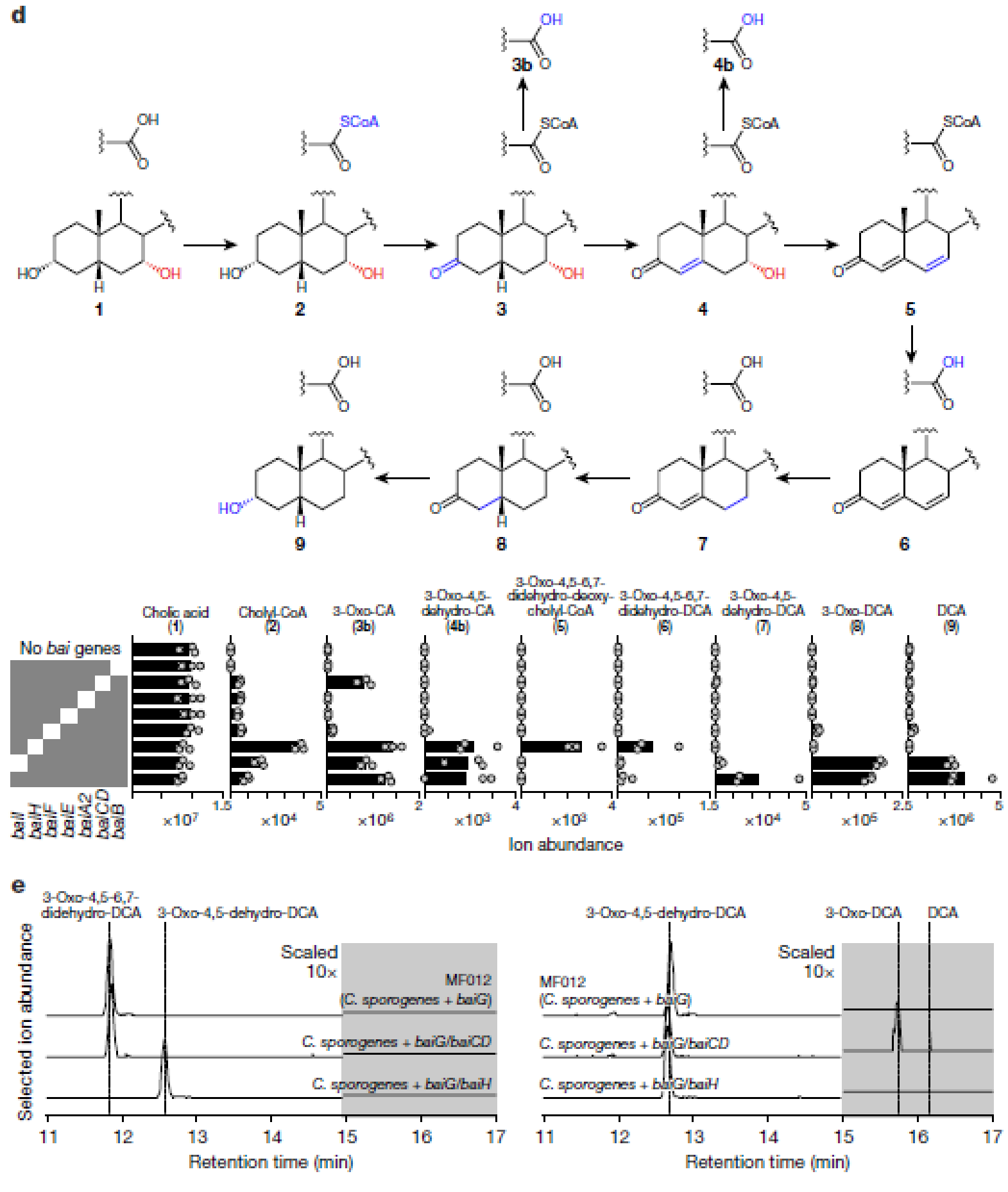
- 为了验证这种非天然的生物合成可能的分支点,又建立了一系列的菌株,对每个菌株进行单个酶的敲除。
Colonizing mice with engineered C. sporogenes
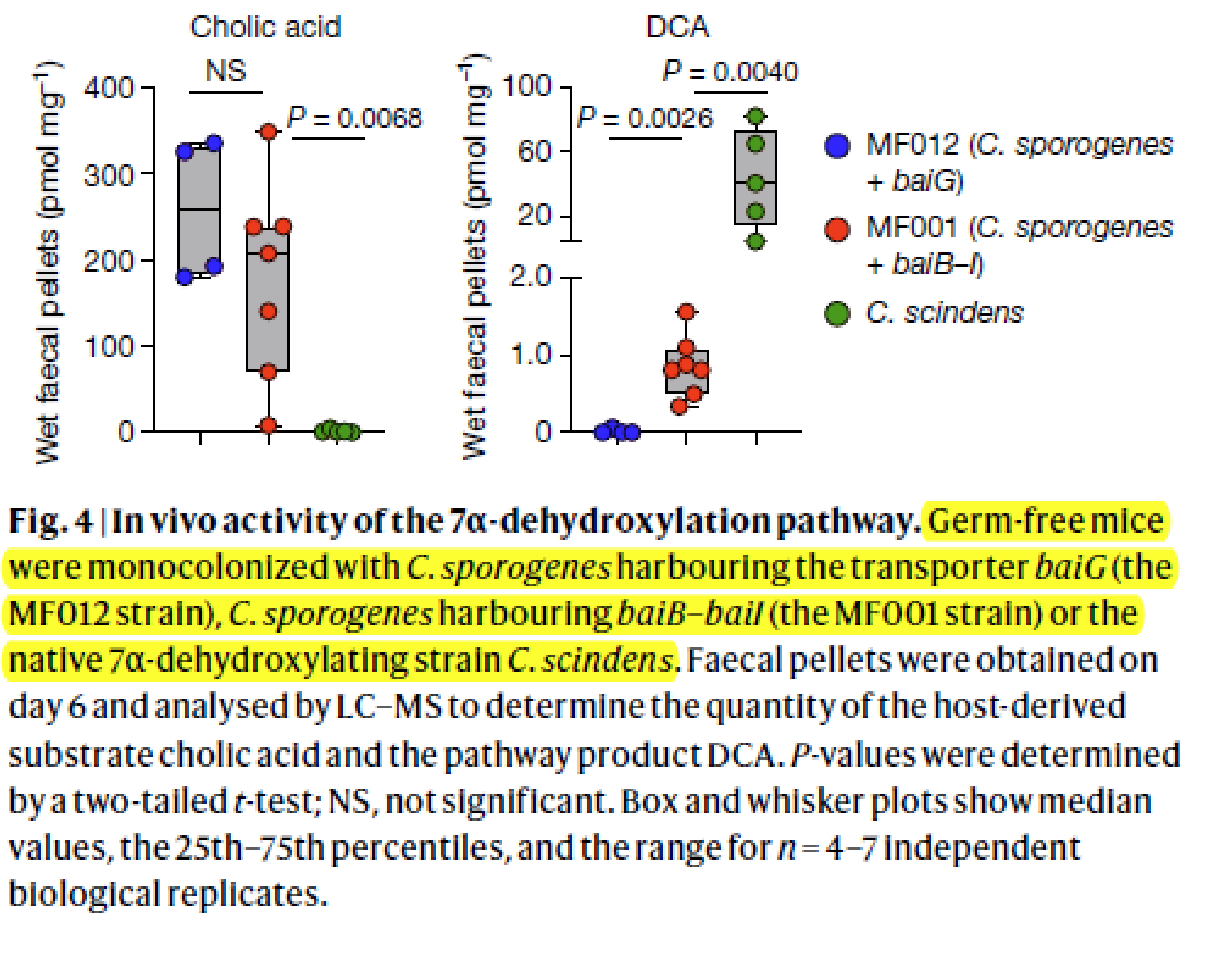
- 将这个改造的菌株MF001定植到小鼠上,去证明这种移植能否使宿主也具备这个合成能力
- Negative control: germ-free mice + C.sporogene baiG (bile acid 的转运体)
- Positive control: germ-free mice + wile-type C scindens (native bai-operon)
- 结果表明确实遗传改造确实让小鼠具备了7-脱羟基的能力,但是水平低于天然,解释原因是猜测可能还有其他的基因有参与,从而使这个pathway的通量增加
讨论:
- 文章展示了完整的7a脱羟基的通路,展示了改造菌株通路的潜力
- 也提及了目前的缺陷:需要更加高效的方法来鉴定已知代谢物和orphan gene cluster之间的通路
- 需要更好的工具将天然菌株定植到肠道,从而产生新的分子
感受
- 整篇文章思路比较清晰也直接,讲清楚了一个通路,然后通过遗产改造展示出潜力
- 值得学习的点:如何有条理的讲清楚一个通路和应用价值




